jun 13, 2022
Philips anuncia los resultados positivos del ensayo clínico TOBA II BTK de su sistema Tack para reparación de disecciones arteriales por debajo de la rodilla
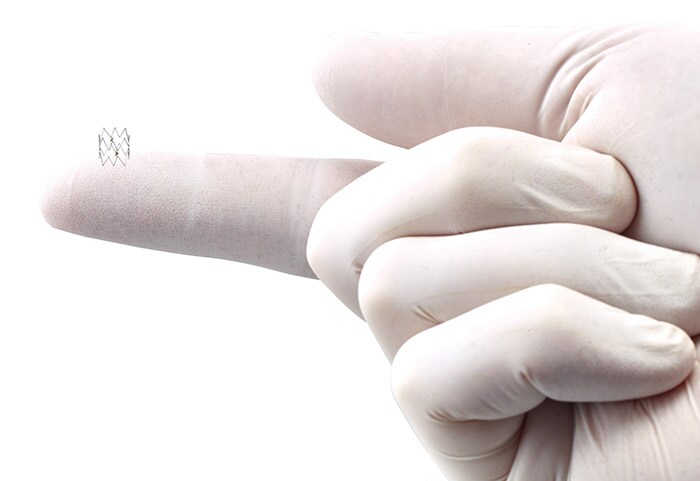
Ámsterdam, 13 de junio de 2022 – Royal Philips, líder mundial en tecnología sanitaria, ha anunciado hoy los últimos resultados del ensayo clínico TOBA II (Tack Optimized Balloon Angioplasty) BTK (below-the-knee), que demuestran que el sistema endovascular Tack (4F) de Philips, el primer y único dispositivo de este tipo aprobado por la FDA, proporciona un efecto de tratamiento continuo y un impacto positivo en la calidad de vida de los pacientes con isquemia crítica de los miembros inferiores, una fase grave de la enfermedad arterial periférica, con datos de hasta tres años con un seguimiento clínico.
La isquemia crítica de los miembros inferiores (ICMI) se produce cuando una obstrucción en una arteria reduce gravemente el flujo sanguíneo, lo que provoca heridas dolorosas, dolor en reposo, úlceras recurrentes e infecciones potencialmente mortales. Si no se trata, el 50% de los pacientes con ICMI sufrirán una amputación o morirán en el primer año [1].
El ensayo TOBA II BTK estudió la seguridad y la eficacia de la reparación de la disección post angioplastia con el sistema endovascular Tack de Philips en pacientes con ICMI y enfermedad infrapoplítea. El sistema endovascular Tack es un dispositivo especializado e implantable para optimizar el tratamiento de las disecciones en pacientes con ICMI. Los criterios de valoración del estudio incluyeron tasas de acontecimientos adversos importantes, la revascularización de la lesión (TLR), la recuperación de la extremidad afectada (TLS) y los parámetros de calidad de vida (QoL).
“Según el seguimiento realizado durante 36 meses en el ensayo TOBA II BTK, en el que se está haciendo un seguimiento a 233 pacientes en 41 centros de todo el mundo, el sistema Tack ofrece un nuevo estándar en la reparación de disecciones arteriales por debajo de la rodilla”, afirma el doctor George Adams, coinvestigador principal del ensayo clínico y director de investigación cardiovascular y vascular en el Hospital Rex de la Universidad de Carolina del Norte en Raleigh. El doctor Adams presentó los resultados del ensayo clínico TOBA II BTK a cientos de cardiólogos y radiólogos intervencionistas y cirujanos vasculares en la conferencia New Cardiovascular Horizons (NCVH) celebrada en Nueva Orleans (EE.UU.) el 2 de junio.
“El dispositivo puede beneficiar significativamente a los pacientes con ICMI cuyo tratamiento con angioplastia con balón suele provocar esta complicación concreta que normalmente no se trata ni se atiende, en detrimento de los resultados clínicos a largo plazo”, añade el doctor Adams.
El análisis a tres años de los resultados de TOBA II BTK incluye los siguientes datos clínicos sobre el sistema endovascular Tack:
Con nuestro sistema endovascular Tack, los intervencionistas pueden reparar de forma fiable las disecciones arteriales por debajo de la rodilla y, al hacerlo, mejorar las tasas de amputación mayor y la calidad de vida de los pacientes”.
Chris Landon
Responsable de negocio de Dispositivos de Terapia Guiada por Imagen de Philips
“En el tratamiento de la enfermedad arterial periférica por debajo de la rodilla con angioplastia con balón, las disecciones de las arterias poplítea, tibial y peronea se producen con una frecuencia considerable”, explica Chris Landon, responsable de negocio de Dispositivos de Terapia Guiada por Imagen de Philips. “Con nuestro sistema endovascular Tack, los intervencionistas pueden reparar de forma fiable las disecciones arteriales por debajo de la rodilla y, al hacerlo, mejorar las tasas de amputación mayor y la calidad de vida de los pacientes”. En ninguno de los dos estudios se registraron acontecimientos adversos importantes hasta los 30 días.
Philips había comunicado previamente los datos de los estudios TOBA II y III, que evaluaron el sistema Tack para la reparación de disecciones de la arteria femoral superficial y poplítea proximal tras una angioplastia con balón no recubierto y/o una angioplastia con balón recubierto de fármaco. Estos ensayos clínicos multicéntricos, mundiales y europeos, demostraron que el uso del sistema endovascular Tack dio lugar a una resolución abrumadora de disección tras la angioplastia con balón no recubierto o con balón recubierto de fármaco.
En conjunto, los ensayos TOBA II, TOBA III y TOBA II BTK respaldan la seguridad y la eficacia del sistema endovascular Tack para la reparación de disecciones tras angioplastia transluminal percutánea en enfermedades arteriales por encima y por debajo de la rodilla. Los datos del ensayo clínico TOBA II BTK a los 36 meses de seguimiento presentados en el NCVH se suman al sólido conjunto de pruebas clínicas que respaldan la seguridad y la eficacia del sistema endovascular Tack en ambas bases vasculares.
El sistema endovascular Tack de Philips está actualmente a la venta en Estados Unidos y en algunos países de la UE. Puede obtener más información, incluida la relativa a la seguridad, aquí. El sistema forma parte de la cartera de productos vasculares periféricos de la compañía, que incluye sistemas avanzados de imagen intervencionista para una guía de precisión, como Vascular Suite en su sistema de terapia guiada por imágenes Azurion; catéteres de ultrasonido intravascular (IVUS) para evaluar la localización de la enfermedad y la morfología de la lesión, así como para guiar y confirmar el tratamiento; dispositivos de aterectomía periférica para eliminar las obstrucciones; balones de esculpido para preparar el vaso; y dispositivos de terapia periférica, como el balón recubierto de fármaco Stellarex, para tratar las lesiones.
Referencias
[1] Hirsh AT, Jaskal ZJ, Hertzer, et al. ACC/AHA 2005 guidelines for the management of patients with peripheral arterial disease (lower extremity, renal, mesenteric, and abdominal aortic): executive summary a collaborative report from the American Association for Vascular Surgery/Society for Vascular Surgery, Society for Cardiovascular Angiography and Interventions, Society for Vascular Medicine and Biology, Society of Interventional Radiology, and the ACC/AHA Task Force on Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Peripheral Arterial Disease) endorsed by the American Association of Cardiovascular and Pulmonary Rehabilitation; National Heart, Lung, and Blood Institute; Society for Vascular Nursing; TransAtlantic Inter-Society Consensus; and Vascular Disease Foundation. J Am Coll Cardiol. 2006 Mar 21;113(11):e463-654.
Sobre Royal Philips
Royal Philips (NYSE: PHG, AEX: PHI) es una empresa líder en tecnologías de la salud, centrada en mejorar la salud y el bienestar de las personas, y facilitar la obtención de mejores resultados en el ciclo de la salud, desde los hábitos saludables y la prevención, hasta el diagnóstico, tratamiento y atención domiciliaria. Philips hace uso de su avanzada tecnología y de sus profundos conocimientos clínicos y del consumidor para ofrecer soluciones integradas. Con sede en los Países Bajos, la compañía es líder en diagnóstico por imagen, terapia guiada por imagen, monitorización de pacientes e informática de la salud, así como en salud del consumidor y atención domiciliaria. Philips registró en 2021 unos ingresos de 17.200 millones de euros y cuenta con aproximadamente 79.000 empleados, con operaciones comerciales y servicios en más de 100 países. Todas las noticias sobre Philips se encuentran en nuestro Centro de noticias.
Topics
Contacts

César García Requena
Brand & Communications Manager Health System Philips Ibérica Tel : +34 91 566 95 25
You are about to visit a Philips global content page
ContinueMedia assets